La enfermedad de Alzheimer (AD) tiene la distinción históricamente única de ser la única enfermedad crónica común sin prevención o curación conocida. Esta proposición se vuelve cada vez más ominosa cuando se considera la creciente marea de Alzheimer que se espera que afecte a Norteamérica y al resto del mundo en las próximas décadas. En los Estados Unidos, 5,3 millones de personas padecen actualmente una enfermedad de Alzheimer (75-80% de todos los casos de demencia), y se espera que este número aumente a 13,8 millones de personas médicamente y económicamente insostenibles para 2050.
La idea de que la EA es recalcitrante para todas las intervenciones se basa en una creencia que ha sido ampliamente refutada en la última década – que el sistema nervioso es estático y categóricamente inmutable. El gran costo y la consistencia de los ensayos fallidos de drogas en las últimas décadas nos llevan a una conclusión central: la enfermedad de Alzheimer es un fenómeno multifactorial que se desarrolla durante varias décadas antes del inicio de los síntomas y es, en gran parte, un resultado del estilo de vida.
Afortunadamente, el concepto de neuroplasticidad se está convirtiendo rápidamente en corriente principal. Un estudio de la UCLA de 2014, aunque pequeño (mejoría en 9 de cada 10 participantes), mostró por primera vez una reversión de la EA leve a moderada utilizando un enfoque integral de recomendaciones de dieta y estilo de vida individualizadas. De todos los factores sistémicos en juego, tal vez ninguno es más crucial para tratar que la resistencia a la insulina.
“DIABETES DEL CEREBRO”
Un hallazgo clave en nuestra evolución de la comprensión de la patología relevante es la fuerte correlación entre la EA y la resistencia a la insulina, el síndrome metabólico y la diabetes tipo 2 (DM2).De hecho, hasta el 40% de la patología de la EA se ha atribuido a la hiperinsulinemia. Los niveles más altos de HbA1c se correlacionan con una menor capacidad cognitiva y cambios en la microestructura del hipocampo, y el estado genético positivo de APOE e4 (el determinante genético más bien estudiado del riesgo de EA) se correlaciona con un mayor riesgo de DM2, alteración de los perfiles lipídicos y enfermedad cardiovascular . Como el metabolismo cerebral de la glucosa de larga duración es un aspecto central de la patología de la EA, la investigación sugiere que la intervención a mediana edad puede ser especialmente crítica para el éxito de los resultados. Además, el abordaje de diabetes con éxito en la vida posterior reduce la conversión de deterioro cognitivo leve a EA y todas las causas de la demencia.
FISIOPATOLOGÍA
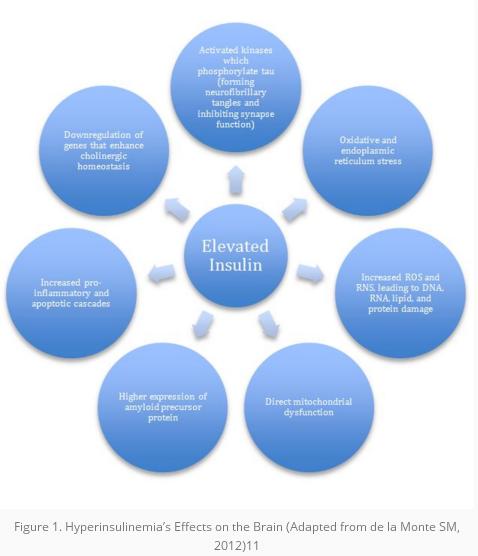
También es bien sabido que las regiones cerebrales (especialmente el hipocampo) que se basan principalmente en la insulina y la señalización del factor de crecimiento similar a la insulina (IGF) son las más vulnerables a la patología de la EA. Las alteraciones en la señalización de insulina / IGF cerebral conducen a una mayor expresión de la proteína precursora amiloide β (AβPP) y a la acumulación de agregados de AβPP-Aβ. 11 Algunos de los mecanismos propuestos, todos los cuales son al menos parcialmente susceptibles a los enfoques naturopáticos, se enumeran en la Figura 1
Un enfoque integral de la EA debe ser multifactorial (Tabla 2), pero la base de cualquier terapia exitosa para la demencia debe comenzar con la dieta. Para EA, la fundación de una dieta acertada debe explicar las anormalidades del azúcar de sangre. El estricto control del azúcar es aún más crucial en la población de edad avanzada, ya que las preferencias gustativas aumentan para los alimentos ricos en calorías y carbohidratos, pobres en micronutrientes.
LA MENTE ES SU DIETA
Se estudió una dieta híbrida mediterránea y DASH (ver Tabla 1), con varias modificaciones cognitivas específicas, en una población de 923 participantes que fueron seguidos durante 4,5 años. Apropiadamente denominada dieta MIND, aquellos que obtuvieron puntajes en el 1/3 más alto de adherencia (estricta adherencia) a la dieta tuvieron una reducción del 53% en el riesgo de desarrollar EA. Igual de impresionante, aquellos que estaban en el medio 1/3 (moderada adherencia) tuvieron una reducción del riesgo del 35%.
Sin embargo, para la mayoría de los pacientes que consultan a un Naturópata, la adhesión a esta dieta no parecerá especialmente estricta; Por ejemplo, se obtuvo una puntuación positiva al limitar la carne roja a un exceso de 4 veces por semana. Además, el índice glucémico de los alimentos consumidos no se consideró mensurable, proporcionando una nueva oportunidad para optimizar la dieta. Aun así, la dieta MIND se asoció con una tasa de declinación cognitiva más lenta equivalente a 7,5 años de edad mental. Si bien el resultado del estudio se relaciona más con la prevención que con el tratamiento, los mismos principios pueden aplicarse a individuos con diagnóstico precoz, ya que los cambios patológicos típicamente ocurren mucho antes de que los síntomas se establezcan.
Tabla 1. Dieta MIND utilizada en el estudio clínico
AYUNO SALUTOGENO
El ayuno salutógeno ha sido durante mucho tiempo un acercamiento de los practicantes higienistas, y se confiando sobradamdamnete en los orígenes de la cura de la naturaleza. En los países industrializados donde la comida (rápida) es fácilmente disponible, la población está comiendo en exceso a ritmos sin precedentes. Una mayor ingesta de calorías y grasas en 980 ancianos estudiados a lo largo de 4 años se asoció con un riesgo de EA 2,3 veces mayor, pero sólo en aquellos que fueron APOE4 +. En un estudio de 18 años, los que habitualmente consumen menos calorías tenían tasas más bajas de EA, y por cada 1.0 aumento en el IMC a los 70 años, el riesgo de EA aumentó en un 36%. En una revisión de los efectos metabólicos de las dietas restringidas en calorías o ayunos intermitentes, la sensibilidad a la insulina mide a través de HOMA-IR se correlacionó bien con la pérdida de peso en la mayoría de los estudios; Un estudio típico correlacionó una pérdida de peso del 8% con una mejora del 33% en la sensibilidad a la insulina. De manera similar, se observaron reducciones en la insulina en ayunas del 20-31% después de 8-12 semanas de tratamiento. En la mayoría de los estudios de ayuno intermitente o alternativo, la pérdida de grasa visceral es paralela a la pérdida de peso general, del orden de 4-7% durante 6-24 semanas de tratamiento.
Aunque actualmente se carece de suficientes estudios de resultados a largo plazo en seres humanos (se han realizado muchos estudios en animales), existen varios ensayos pequeños. La restricción calórica (CR) de 3-4 meses mejoró la función cognitiva en los ancianos, medida por las puntuaciones de la memoria verbal, en paralelo con la reducción de la insulina en ayuna y la proteína C reactiva (CRP).
Existen varios mecanismos celulares potenciales implicados en estas dietas (pensados principalmente como resultado del efecto hormonal de la restricción energética), los más estudiados incluyen la reducción del estrés oxidativo, la mejora de la bioenergética celular, la mejora de la señalización del factor neurotrófico (BDNF y FGF2) Inflamación (TNFα reducido, IL-1β e IL-6). Aunque existen muchas variaciones de restricción calórica y ayuno intermitente, se espera mayor cumplimiento y perfiles de seguridad con ayunos diarios durante la noche (que van desde un mínimo de 12 horas a 16 o 18 horas) en comparación con ayunos más largos. Por supuesto, cada paciente debe ser evaluado sobre una base individual y cuidadosamente monitoreado durante el tratamiento.
DIETAS CETOGÉNICAS
Otro beneficio clave del ayuno intermitente o restricción calórica es la inducción de cetosis después de 12-16 horas de ayuno. El hipometabolismo de la glucosa (que conduce a la privación crónica de la energía del cerebro) en pacientes con EA es aproximadamente un 20-25% menor que en los individuos cognitivamente normales. En aquellos propensos a la diabetes, estos cambios son a menudo más pronunciado en la corteza frontal, y en algunas se pueden descubrir a edades tan jóvenes como de 24 años. Es importante destacar que la capacidad de producir y utilizar los cuerpos cetónicos como un sustrato alternativo en realidad pueden aumentar con la edad y con resistencia a la insulina (que provoca un aumento en los transportadores de monocarboxilato). Aunque sólo tenemos 33 g / día de glucosa en las reservas de glucógeno, el cerebro humano medio metaboliza 110-145 g / día de glucosa para la producción de ATP. Por esta razón, una fuente de combustible alternativo es necesaria y afortunadamente proporcionada por la naturaleza: los cuerpos cetónicos (específicamente beta-hidroxibutirato y acetoacetato, que son beta-oxidados en el hígado de ácidos grasos de cadena larga).
Las dietas cetogénicas tienden a ser altas en grasa y restrictivas de los carbohidratos. Un perfil común de macronutrientes incluiría un máximo de 30 g de carbohidratos, 1 g de proteína / kg de peso corporal y el resto de calorías de grasa (20% saturado / 80% poliinsaturado y monoinsaturado). Una alternativa que es probable que cumpla con un mayor cumplimiento es el consumo directo de triglicéridos de cadena media (TCM), más fácilmente disponibles en el aceite de coco, que aumentan los niveles de cetonas sin tener en cuenta la ingesta de macronutrientes; Los aceites de TCM proporcionan una relación dosis-respuesta lineal a cetonas plasmáticas aumentadas. Una dosis terapéutica es de 2 cucharadas de aceite de coco virgen orgánico al día, que proporciona en promedio 20 g de TCM. Esta dosis debe valorarse gradualmente para evitar trastornos digestivos. De otro modo, se ha demostrado que los aceites TCM son seguros, con un tratamiento de 30 días de TCM de 30 g / día sin afectar adversamente el peso corporal, el contenido de grasa corporal, el índice de masa corporal, la glucosa en suero, la insulina, los triglicéridos, el colesterol o los ácidos grasos libres.
La verdadera enfermedad de Alzheimer familiar es extremadamente rara, y aunque hay un componente genético (estado positivo de APOE4), este efecto puede ser mitigado con un enfoque Naturopático. EA es, por supuesto, una enfermedad que se manifiesta en la patología cerebral de órgano final. Visto de esta manera reduccionista, es probable que continúe siendo una carga que afecta cada vez más al mundo industrializado. Sin embargo, si se aborda como una enfermedad sistémica con susceptibilidad específica del cerebro , tal vez la profesión naturopática puede estar a la vanguardia de preservar todo lo que está en juego.
Tabla 2. Un enfoque multifactorial de la enfermedad de Alzheimer
Intervención Resultados del estudio
Vitamina E 2000 IU / d alfa-tocoferol retrasó la progresión clínica de 19% al año en comparación con placebo en leve a moderada AD
La deficiencia severa (<25 nmol / L) se asoció con un riesgo aumentado del 122% de demencia de todas las causas; Y la deficiencia (25-50 nmol / L) se asoció con un aumento del 51% de riesgo
B Vitaminas / El tratamiento con complejo B en sujetos con
La atrofia cerebral (& homocisteína> 13 μmol / L) fue 53% menor en el grupo de tratamiento con vitamina B activa
La calidad de las relaciones parece más importante que la cantidad
Participación cognitiva. La historia de la actividad cognitiva de por vida puede apoyar un mejor rendimiento cognitivo; Esta relación está mediada por un mecanismo independiente de la carga Aβ 35
Toxicidad ambiental Los metales neurotóxicos como el plomo, el mercurio, el aluminio, el cadmio y el arsénico, así como algunos plaguicidas y nanopartículas basadas en metales, han participado en la AD debido a su capacidad para aumentar el péptido Aβ y la fosforilación de P-Tau
(25OHD = 25-hidroxivitamina D, Aβ = beta-amiloide, P-Tau = proteína tau, MMSE = Mini-Examen del Estado Mental)
- Alzheimer’s Association. Alzheimer’s disease facts and figures. Alzheimers Dement. 2015;11(3):332-384.
- Bredesen DE. Reversal of cognitive decline: a novel therapeutic program. Aging (Albany NY). 2014;6(9):707-717.
- Biessels GJ, Staekenborg S, Brunner E, et al. Risk of dementia in diabetes mellitus: a systematic review. Lancet Neurol. 2006;5(1):64-74.
- Kopf D, Frolich L. Risk of incident Alzheimer’s disease in diabetic patients: a systematic review of prospective trials. J Alzheimers Dis. 2009;16(4):677-685.
- Kerti L, Witte AV, Winkler A, et al. Higher glucose levels associated with lower memory and reduced hippocampal microstructure. 2013;81(20):1746-1752.
- El-Lebedy D, Raslan HM, Mohammed AM. Apolipoprotein E gene polymorphism and risk of type 2 diabetes and cardiovascular disease. Cardiovasc Diabetol. 2016;15:12.
- Willette AA, Bendlin BB, Starks EJ, et al. Association of Insulin Resistance With Cerebral Glucose Uptake in Late Middle-Aged Adults at Risk for Alzheimer Disease. JAMA Neurol. 2015;72(9):1013-1020.
- Cooper CC, Sommerlad A, Lyketsos CG, Livingston G. Modifiable predictors of dementia in mild cognitive impairment: a systematic review and meta-analysis. Am J Psychiatry. 2015;172(4):323-334.
- de la Monte SM, Wands JR. Review of insulin and insulin-like growth factor expression, signaling, and malfunction in the central nervous system: relevance to Alzheimer’s disease. J Alzheimers Dis. 2005;7(1):45-61.
- Freude S, Schilbach K, Schubert M. The role of IGF-1 receptor and insulin receptor signaling for the pathogenesis of Alzheimer’s disease: from model organisms to human disease. Curr Alzheimer Res. 2009;6(3):213-223.
- de la Monte SM. Contributions of Brain Insulin Resistance and Deficiency in Amyloid-Related Neurodegeneration in Alzheimer’s Disease. Drugs. 2012;72(1):49-66.
- Mundas D, Cooper JK, Weiler PG, et al. Dietary preference for sweet foods for patients with dementia. J Am Geriatr Soc. 1990;38(9):999-1007.
- Morris MM, Tangney CC, Wang Y, et al. MIND diet associated with reduced incidence of Alzheimer’s disease.Alzheimers Dement. 2015;11(9):1007-1014.
- Luchsinger JA, Tang MX, Shea S, Mayeux R. Caloric intake and the risk of Alzheimer disease. Arch Neurol. 2002;59(8):1258-1263.
- Gustafson D, Rothenberg E, Blennow K, et al. An 18-year follow-up of overweight and risk of Alzheimer disease.Arch Intern Med. 2003;163(13):1524-1528.
- Barnosky AR, Hoddy KK, Unterman TG, Varady KA. Intermittent fasting vs daily calorie restriction for type 2 diabetes prevention: a review of human findings. Transl Res. 2014;164(4):302-311.
- Witte AV, Fobker M, Gellner R, et al. Caloric restriction improves memory in elderly Proc Natl Acad Sci U S A. 2009;106(4):1255-1260.
- Mattson MP. Energy intake and exercise as determinants of brain health and vulnerability to injury and disease.Cell Metab. 2012;16(6):706-722.
- Arumugam TV, Phillips TM, Cheng A, et al. Age and energy intake interact to modify cell stress pathways and stroke outcome. Ann Neurol. 2010;67(1):41-52.
- Cunnane S, Nugent S, Roy M, et al. Brain fuel metabolism, aging, and Alzheimer’s disease. 2011;27(1):3-20.
- Castellano CA, Baillargeon JP, Nugent S, et al. Regional brain glucose hypometabolism in young women with polycystic ovary syndrome: possible link to mild insulin resistance. PLoS One. 2015;10(12):e0144116.
- London ED, Margolin RA, Duara R, et al. Effects of fasting on ketone body concentrations in healthy men of different ages. J Gerontol. 1986;41(5):599-604.
- Robinson AM, Williamson DH. Physiological roles of ketone bodies as substrates and signals in mammalian tissues. Physiol Rev. 1980;60(1):143-187.
- Cunnane SC, Courchesne-Loyer A, St-Pierre V, et al. Can ketones compensate for deteriorating brain glucose uptake during aging? Implications for the risk and treatment of Alzheimer’s disease. Ann N Y Acad Sci. 2016;1367(1):12-20.
- Courchesne-Loyer A, Fortier M, Tremblay-Mercier J, et al. Stimulation of mild, sustained ketonemia by medium-chain triacylglycerols in healthy humans: estimated potential contribution to brain energy metabolism.Nutrition. 2013;29(4):635-640.
- Dysken MW, Sano M, Asthana S, et al. Effect of vitamin E and memantine on functional decline in Alzheimer disease: the TEAM-AD VA cooperative randomized trial. JAMA. 2014;311(1):33-44.
- Littlejohns TJ, Henley WE, Lang IA, et al. Vitamin D and the risk of dementia and Alzheimer disease. Neurology. 2014;83(10):920-928.
- Yurko-Mauro K, Alexander DD, Van Elswyk ME. Docosahexaenoic acid and adult memory: a systematic review and meta-analysis. PLoS One. 2015;10(3):e0120391.
- Yurko-Mauro K, McCarthy D, Rom D, et al. Beneficial effects of docosahexaenoic acid on cognition in age-related cognitive decline. Alzheimers Dement. 2010;6(6):456-464.
- de Jager CA, Oulhaj A, Jacoby R, et al. Cognitive and clinical outcomes of homocysteine-lowering B-vitamin treatment in mild cognitive impairment: a randomized controlled trial. Int J Geriatr Psychiatry. 2012;27(6):592-600.
- Smith AD, Smith SM, de Jager CA, et al. Homocysteine-lowering by B vitamins slows the rate of accelerated brain atrophy in mild cognitive impairment: a randomized controlled trial. PLoS One. 2010;5(9):e12244.
- Wells RE, Yeh GY, Kerr CE, et al. Meditation’s impact on default mode network & hippocampus in mild cognitive impairment: a pilot study. Neurosci Lett. 2013;556:15-19.
- Foubert-Samier A, Le Goff M, Helmer C, et al. Change in leisure and social activities and risk of dementia in elderly cohort. J Nutr Health Aging. 2014;18(10):876-882.
- Amieva H, Stoykova R, Matharan F, et al. What aspects of social network are protective for dementia? Not the quantity but the quality of social interactions is protective up to 15 years later. Psychosom Med. 2010;72(9):905-911.
- Gidicsin CM, Maye JE, Locascio JJ, et al. Cognitive activity relates to cognitive performance but not to Alzheimer disease biomarkers. Neurology. 2015;85(1):48-55.
- Groot C, Hooghiemstra AM, Raijmakers PJ, et al. The effect of physical activity on cognitive function in patients with dementia: A meta-analysis of randomized control trials. Ageing Res Rev. 2016;25:13-23.
- Chin-Chan M, Navarro-Yepes J, Quintanilla-Vega B. Environmental pollutants as risk factors for neurodegenerative disorders: Alzheimer and Parkinson diseases. Front Cell Neurosci. 2015;9:124.
- Zhou J, Peng W, Xu M, et al. The effectiveness and safety of acupuncture for patients with Alzheimer disease: a systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore). 2015;94(22):e933.
- Wade AG, Farmer M, Harari G, et al. Add‐on prolonged‐release melatonin for cognitive function and sleep in mild to moderate Alzheimer’s disease: a 6‐month, randomized, placebo controlled, multicenter trial. Clin Interv Aging. 2014;9:947-
Fuente: ndnr
Etiquetas: Investigaciones Naturopáticas